Indice dell’articolo
- Malattie cerebrovascolari acute: gestione medico-infermieristica
- Piano assistenziale infermieristico delle malattie cerebrovascolari
Malattie cerebrovascolari acute: gestione medico-infermieristica
Le MCV predominano nell’età media-avanzata e il rischio di avere una malattia cerebrovascolare raddoppia ogni decade a partire dai 55 anni. L’ictus nei Paesi occidentali costituisce la terza causa di morte e la prima causa di invalidità permanente.
In Occidente le MCV ischemico-infartuali costituiscono la grande maggioranza essendo l’85-90% di tutti i casi; nei Paesi asiatici gli eventi emorragici sono relativamente più frequenti.
In questi ultimi anni si è assistito ad una riduzione della morbilità e mortalità per patologia cerebrovascolare dovuta ad un migliore controllo e trattamento delle patologie
predisponenti, ad un’aumentata capacità diagnostica (migliorata sensibilità delle tecniche neuroradiologiche e maggiore diffusione delle stesse anche in centri periferici)
ed infine ad un più adeguato trattamento del paziente con malattia cerebrovascolare (terapia più tempestiva nel paziente acuto e maggiore attenzione alla rieducazione funzionale nel paziente con esiti). Tuttavia, considerato il progressivo invecchiamento della popolazione, il numero assoluto di MCV è in aumento.
Guida al monitoraggio in Area Critica
Il monitoraggio è probabilmente l’attività che impegna maggiormente l’infermiere qualunque sia l’area intensiva in cui opera.Non può esistere area critica senza monitoraggio intensivo, che non serve tanto per curare quanto per fornire indicazioni necessarie ad agevolare la decisione assistenziale, clinica e diagnostico-terapeutica, perché rilevando continuamente i dati si possono ridurre rischi o complicanze cliniche.Il monitoraggio intensivo, spesso condotto con strumenti sofisticati, è una guida formidabile per infermieri e medici nella cura dei loro malati. La letteratura conferma infatti che gli eventi avversi, persino il peggiore e infausto, l’arresto cardiocircolatorio, non sono improvvisi ma solitamente vengono preannunciati dal peggioramento dei parametri vitali fin dalle 6-8 ore precedenti.Il monitoraggio è quindi l’attività “salvavita” che permette di fare la differenza nel riconoscere precocemente l’evento avverso e migliorare i risultati finali in termini di morbilità e mortalità.Riconosciuto come fondamentale, in questo contesto, il ruolo dell’infermiere, per precisione, accuratezza, abilità nell’uso della strumentazione, conoscenza e interpretazione dei parametri rilevati, questo volume è rivolto al professionista esperto, che mette alla prova nelle sue conoscenze e aggiorna nel suo lavoro quotidiano, fornendo interessanti spunti di riflessione, ma anche al “novizio”, a cui permette di comprendere e di utilizzare al meglio le modalità di monitoraggio. A cura di:Gian Domenico Giusti, Infermiere presso Azienda Ospedaliero Universitaria di Perugia in UTI (Unità di Terapia Intensiva). Dottore Magistrale in Scienze Infermieristiche ed Ostetriche. Master I livello in Infermieristica in anestesia e terapia intensiva. Professore a contratto Università degli Studi di Perugia. Autore di numerose pubblicazioni su riviste italiane ed internazionali. Membro del Comitato Direttivo Aniarti.Maria Benetton, Infermiera presso Azienda ULSS 9 di Treviso. Tutor Corso di laurea in Infermieristica e Professore a contratto Università degli Studi di Padova. Direttore della rivista “SCENARIO. Il nursing nella sopravvivenza”. Autore di numerose pubblicazioni su riviste italiane. Membro del Comitato Direttivo Aniarti.
a cura di Gian Domenico Giusti e Maria Benetton | 2015 Maggioli Editore
15.00 € 14.25 €
Classificazione e eziopatogenesi delle malattie cerebrovascolari
Diversi eventi patologici sono causa dell’ischemia cerebrale o dell’emorragia intracerebrale.
Nella Tabella 1 e 2 riportiamo una classificazione etio-patogenetica delle MCV.
Ischemia-infarto cerebrale
Tab. 1 – Classificazione delle malattie cerebrovascolari ischemiche
| Patogenesi | Etiologia |
|---|---|
| Occlusione trombotica | a) Aterosclerosi (sedi preferite biforcazioni e tortuosità grossi vasi) b) Lipoialinosi (piccole arterie e arteriole dei gangli della base, ponte, talamo, sostanza bianca emisferica, cervelletto) con conseguente formazione dei microaneurismi di Charcot e Bouchard c) Vasculiti (arterite temporale, poliarterite nodosa, granulomatosi di Wegener, sifilide) d) Dissezioni arteriose (carotide, vertebrale, aa. intracraniche) spontanee o traumatiche e) Patologie ematologiche (policitemia, trombocitosi, CID, emoglobinopatie) f) Varie (cocaina, amfetamine) |
| Occlusione embolica | a) Origine cardiaca b) Origine aterotromboembolica arteriosa c) Origine sconosciuta (associata ad uno stato di ipercoagulabilità, neoplasie) |
| Vasocostrizione | a) Vasospasmo da ESA b) Vasocostrizione reversibile |
Emorragia intracranica
Tab. 2 – Classificazione delle malattie cerebrovascolari emorragiche
| Patogenesi | Etiologia |
|---|---|
| Emorragia intracerebrale | a) Ipertensiva (rottura spontanea di una piccola arteria penetrante nella profondità degli emisferi cerebrali) b) Angiopatia amiloide (degenerazione delle arteriole con deposizione di amiloide) nelle emorragie lobari c) Malformazioni arterovenose (MAV), aneurismi, tumori, diatesi emorragica, malattie ematologiche, uso di cocaina |
| Emorragia subaracnoidea | d) Rottura aneurisma sacculare, micotico e) Sanguinamento da una MAV f) Estensione nello spazio subaracnoideo di una emorragia primitivamente intracerebrale g) Post-traumatica |
| Ematoma epidurale | Post-traumatico |
| Ematoma subdurale | Solitamente post-traumatico |
Definizioni
Da un punto di vista clinico distinguiamo l’ictus dall’attacco ischemico transitorio; la
differenza sostanziale tra le due sindromi è la durata del quadro clinico (lo spartiacque
sono le 24 ore), tempo che è stato arbitrariamente scelto nel 1978 dall’Organizzazione
Mondiale della Sanità.
La diagnosi di TIA/ictus è quindi sempre basata sulla clinica. L’attacco ischemico transitorio (TIA, acronimo inglese) è una sindrome clinica caratterizzata dalla comparsa di un improvviso deficit neurologico focale e/o monoculare, di natura ischemica e della durata inferiore alle 24 ore (la maggioranza dei TIA si risolvono entro un’ora).
L’ictus è una sindrome clinica caratterizzata dalla comparsa rapida di sintomi e/o segni della durata superiore alle 24 ore (o che causa la morte del paziente), dovuti ad un
deficit neurologico di solito focale (può essere globale nei pazienti in coma profondo o
con ESA) a genesi vascolare, non traumatica.
Non esiste una stretta correlazione tra quadro clinico e anatomo-patologico; infatti
mentre l’ictus si associa sempre ad infarto cerebrale, il TIA può non essere dovuto solo
ad una ischemia transitoria senza conseguente morte cellulare (infatti il 13% dei TIA si
associa ad un infarto silente).
Inchiesta anamnestica
La raccolta dell’anamnesi rappresenta sempre il primo passo nella valutazione del
paziente, spesso è l’unico elemento diagnostico, deve riguardare tutti gli elementi necessari a definire le caratteristiche del quadro clinico (Tab. 4) e se possibile deve avvalersi anche degli elementi che possono fornire gli eventuali testimoni dell’accaduto (per esempio i familiari). È importante innanzitutto indagare se vi sono fattori di rischio (Tab. 3) per patologia vascolare:
- Età (non modificabile)
- Sesso (preferenza del sesso maschile solo prima dei 50 anni, non modificabile)
- Ipertensione arteriosa (principale fattore di rischio modificabile con la terapia)
- Precedenti TIA/ictus (non modificabile con la terapia)
- Cardiopatie (causa di embolie, parzialmente modificabile con la terapia)
- Diabete (parzialmente modificabile con la terapia)
- Uso di contraccettivi
Tab. 3 – Fattori di rischio
| Anamnesi patologica remota | Pregresso TIA/ictus; Ipertensione, diabete, dislipidemie, malattie cardiovascolari |
| Anamnesi familiare | MCV, malattie cardiovascolari, diabete |
| Abitudini di vita | Fumo, vita sedentaria, abuso di sostanze, alcool, dieta |
Identificazione dei sintomi nelle malattie cerebrovascolari
La valutazione del paziente con sospetta MCV si articola su sei elementi cardine che
possiamo riassumere nelle seguenti domande:
- È un sospetto ictus? (a tal fine si possono utilizzare delle scale di valutazione, per
esempio vedi Tab. 5) - Quando sono iniziati i segni neurologici?
- Il paziente è cosciente?
- È un evento ischemico o emorragico?
- Se è un ictus: è un ictus lacunare (miglior prognosi) o a localizzazione carotidea o
vertebro-basilare? - Quanto è grave il danno neurologico?
Tab. 4 – Caratteristiche dell’evento ictale
| Modalità d’esordio | – Improvviso – Con prodromi |
| Durata | – Definire l’ora di esordio dei sintomi – Quanto è durata la sintomatologia – Sono ancora presenti i sintomi/segni |
| Sede | – Quale parte/i del corpo o delle funzioni è/sono colpita/e |
| Qualità | a) Le alterazioni sono focali o diffuse b) Le alterazioni sono “negative” (deficit di una funzione) o “positive” (allucinazioni, formicolii, movimenti involontari ripetuti) c) Le alterazioni sono definite sin dall’esordio o si sono intensificate/progredite verso altre parti del corpo |
| Sintomi di Accompagnamento | Cefalea, sincope, vomito, crisi epilettica, sintomi cardiologici, ecc. |
Per completare l’anamnesi è sempre fondamentale conoscere i farmaci assunti.
È importante sottolineare che nel TIA/ictus abitualmente l’esordio della sintomatologia
è improvviso, le alterazioni sono focali e “negative” (ovvero determinano la riduzione di una funzione) e la loro manifestazione è già massima sin dall’inizio; più raramente il quadro clinico può peggiorare progressivamente o “a gradini” e allora si parla di ictus in crescendo.
Infine la natura dei sintomi neurologici (caratteristiche e sede del deficit) riflette l’area del cervello che è ischemica/infartuata o lesionata dall’emorragia o dall’edema; infatti talvolta alcuni sintomi/segni sono esclusivi di alcune zone. Le MCV si possono manifestare con sintomi neurologici generali e focali.
Sono sintomi neurologici generali:
- Alterazioni dello stato di vigilanza/coscienza
- Cefalea improvvisa ed importante
- Lipotimia/sincope
- Convulsioni
- Perdita del controllo sfinteriale
- Alterazioni del respiro
Sono sintomi neurologici focali:
- Segni motori
- Territorio carotideo. Paresi (calo di forza), plegia (impossibilità al movimento) di una parte (per esempio di un arto) o dell’intero emilato del corpo
- Territorio vertebro-basilare. Paraparesi/paraplegia (calo di forza bilaterale),
tetraparesi/tetraplegia (di tutti e quattro gli arti) - Territorio vertebro-basilare. Disfagia (difficoltà a deglutire)
- Disfagia (difficoltà a deglutire). Atassia (perdita di equilibrio)
- Sintomi sensitivi
- Somatosensoriali
- Territorio carotideo. Alterata sensibilità in una parte o in un emilato del
corpo
- Territorio carotideo. Alterata sensibilità in una parte o in un emilato del
- Visivi
- Territorio carotideo. Amaurosi fugax (perdita completa o parziale della
vista in un occhio) - Territorio carotideo/vertebro-basilare. Emianopsia (perdita della vista nella metà del campo visivo), quadrantopsia (perdita della vista in un quadrante del campo visivo)
- Territorio vertebro-basilare. Cecità bilaterale
- Territorio vertebro-basilare. Diplopia.
- Territorio carotideo. Amaurosi fugax (perdita completa o parziale della
- Alterazioni del linguaggio
- Disfasia (difficoltà a comprendere il linguaggio parlato o a esprimerlo)
- Dislessia (difficoltà a leggere)
- Disgrafia (difficoltà a scrivere)
- Discalculia (difficoltà ad eseguire calcoli)
- Disartria (eloquio impastato)
- Sintomi vestibolari
- Territorio vertebro-basilare. Vertigini
- Sintomi cognitivi
- Amnesia
- Difficoltà a svolgere azioni semplici atte ad accudire alla propria persona (vestirsi, pettinarsi, lavarsi i denti)
- Disorientamento temporo-spaziale
- Somatosensoriali
È importante sottolineare che alcuni dei sintomi/segni suelencati (paraparesi, quadraparesi, disfagia, atassia, tinnito, diplopia, disartria, vertigini, amnesia) solo se si presentano in combinazione tra loro o con altri sintomi neurologici focali sono espressione di una disfunzione focale.
Abitualmente i deficit colpiscono un emilato; se il deficit è crociato bisogna pensare ad una lesione del tronco encefalico o a lesioni multifocali.
Valutazione del paziente con sospetta malattia cerebrovascolare
Una valutazione del paziente con sospetta MCV è quella ottenuta con il “Cincinnati pre-hospital stroke scale” (Tab. 5). Questa scala è stata pensata proprio per il paziente
cosciente con sospetto ictus e permette una facile e rapida valutazione degli eventuali
deficit presenti.
Tab. 5 – Cincinnati pre-hospital stroke scale
| PARESI FACCIALE: chiedere al paziente di sorridere e mostrare i denti (valuta se i due emivolti si muovono in maniera simmetrica) |
| DEFICIT MOTORIO ARTI SUPERIORI: chiedere al paziente di estendere entrambi gli arti superiori per 10” mentre tiene gli occhi chiusi (valuta se entrambi gli arti si muovono e mantengono la posizione in maniera simmetrica) |
| DEFICIT MOTORIO ARTI INFERIORI: chiedere al paziente di estendere entrambi gli arti inferiori per 10” mentre tiene gli occhi chiusi (valuta se entrambi gli arti si muovono e mantengono la posizione in maniera simmetrica) |
| ALTERAZIONI DEL LINGUAGGIO: chiedere al paziente di ripetere una frase (es: “trecentotrentatreesimo reggimento di cavalleria”) (valuta se parla e se usa le parole correttamente e con linguaggio fluente) |
Invece, la valutazione della Glasgow Coma Scale (GCS – Tab. 6) è utile per quantificare la severità del danno neurologico soprattutto nel paziente con alterazione della coscienza (in particolare nel paziente con ictus emorragico dove il quadro può evolvere
rapidamente).
Tab. 6 – Glasgow Coma Scale
| 1 | 2 | 3 | 4 | 5 | 6 | |
| Apertura occhi | Non apre gli occhi | allo stimolo doloroso | Alla chiamata | spontanea | N/A | N/A |
| Risposta verbale | Non risponde | Con suoni incomprensibili | Con parole senza senso | confusa | appropriata | N/A |
| Risposta motoria | Non reagisce | Estende l’arto stimolato con il dolore (decerebrazione) | Flette l’arto stimolato con il dolore (decorticazione) | Allontana la parte dallo stimolo doloroso | Localizza il dolore e cerca di allontanarlo | Esegue ordini semplici |
Il quadro clinico può variare da un’alterazione focale di lieve entità (per esempio una paresi di un arto) ad un quadro severo per la presenza di turbe della coscienza con gravi deficit motori ed alterazioni cardiorespiratorie, che mettono il Paziente a rischio di vita.
Uno stato di coma è di solito dovuto o ad una emorragia massiva o all’occlusione dell’arteria cerebrale media o ad un arresto cardiaco con ischemia cerebrale globale, ma è assolutamente necessario escludere un’overdose da farmaci o da sostanze psicoattive, gravi alterazioni metaboliche (come l’ipoglicemia o il coma iperosmolare), una crisi epilettica, una sepsi, un trauma cranio-cervicale o l’isteria.
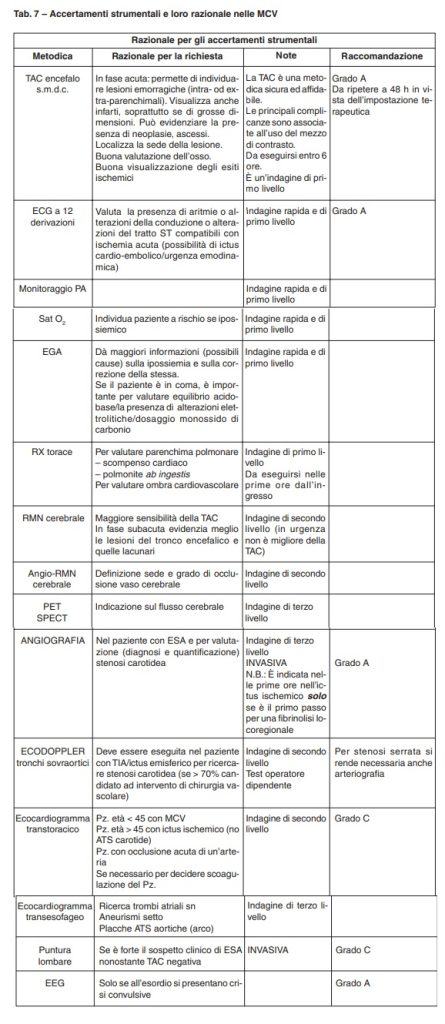
Accertamenti strumentali nelle malattie cerebrovascolari
Tab. 7 – Accertamenti strumentali e loro razionale nelle MCV
Accertamenti di laboratorio
Tab. 8 – Accertamenti di laboratorio e principali motivazioni della loro richiesta
| Esame | Razionale della richiesta | Note |
|---|---|---|
| Emocromo completo | Esclude anemia, policitemia, leucosi. Utile nella flogosi acuta | |
| Glicemia | Per escludere severe alterazioni metaboliche | 1° controllo con stick. Controlli ripetuti in caso di correzione. L’ipoglicemia può dare sia alterazioni dello stato di coscienza sia deficit neurologici focali |
| Creatinina | Per escludere severe alterazioni renali |
|
| Elettroliti plasmatici | Per escludere severe alterazioni dell’equilibrio idro-elettrolitico |
Ricontrollare se in corso infusioni |
| Esame urine | Per escludere patologie internistiche |
|
| Troponina I o T | Rappresenta un marker di necrosi cardiaca di elevata sensibilità e specificità |
Solo in caso di sospetto di concomitante insufficienza coronarica acuta |
| PCR | Elevata in caso di flogosi | |
| Esami tossicologici | Gli esami tossicologici devono essere eseguiti nei pazienti in coma, ove si sospetti un effetto tossico di qualche sostanza |
Terapia delle malattie cerebrovascolari in fase acuta
Obiettivo del trattamento in urgenza del paziente con MCV è:
- forme emorragiche = mantenimento delle funzioni vitali, controllo dell’edema cerebrale, regolazione della pressione arteriosa (PA) e valutazione neurochirurgica
- forme ischemiche = mantenimento delle funzioni vitali, regolazione della PA ed eventuale controllo dell’edema cerebrale
Spesso il paziente con ictus ha valori pressori elevati e ciò può essere dovuto ad una
sottostante ipertensione, ad una reazione da stress all’evento neurologico acuto o ad
una risposta fisiologica ad una ridotta/alterata perfusione cerebrale. Comunque, rilevare valori elevati di pressione arteriosa in corso di MCV non è un’emergenza ipertensiva, a meno che non coesistano altre emergenze mediche come la dissezione aortica, l’infarto miocardico acuto, lo scompenso cardiaco congestizio severo e l’encefalopatia ipertensiva.
La seguente flow chart (Fig. 1) è pensata all’interno del setting dell’emergenza, individuando i primi gesti e le prime tecniche diagnostiche nel paziente con sospetto grave ictus.
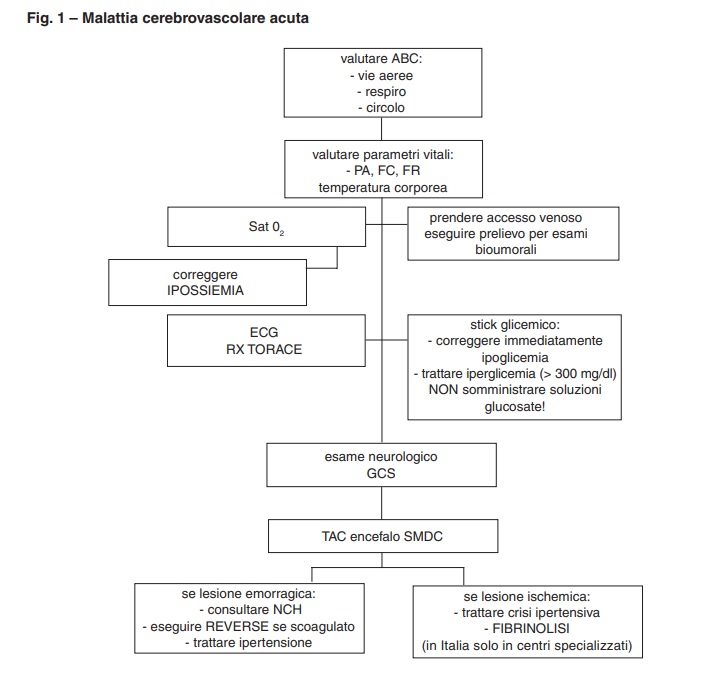
Nel setting dell’emergenza la terapia deve essere di supporto delle funzioni vitali (quando
necessario) e deve trattare quei fattori che peggiorano l’outcome del paziente.
Tab. 9 – Terapia delle MCV
| Intervento | Note e grado di raccomandazione |
|---|---|
| Mantenere il capo sollevato a 30° | Riduce aumento pressione intracranica. Grado C |
| Accesso venoso; Infusione di liquidi isotonici (soluzione fisiologica, Ringer lattato) a 50 ml/h | MAI infusioni rapide perché aumenta il rischio di edema cerebrale (eccetto nel paziente ipoteso). Grado C |
| Intubazione | Se Pz. è in coma (GCS <= 8) Se è necessario proteggere le vie aeree |
| Ossigenoterapia | Se Sat O2 è < 92%. Grado A |
| – Infusione liquidi isotonici – Dopamina EV |
La correzione dell’ipertensione severa deve essere lenta per non determinare una riduzione della pressione di perfusione cerebrale e deve sempre associarsi ad un attento monitoraggio neurologico. Nell’ictus ischemico rimandare trattamento se: PA sistolica è fra 185 e 220mmHg e PA diastolica fra 105 e 120 mmHg. Nell’ictus emorragico trattare tutti i pazienti con PA sistolica >180 mm Hg e diastolica > 105 mm Hg. Grado C |
| Paracetamolo | Mantenere la temperatura corporea < 37°C. Grado C |
| Glucosio (+ tiamina) | Sempre e solo in caso di ipoglicemia (se presente malnutrizione o abuso alcool). Grado C |
| Insulina rapida | Nell’ictus ischemico se glicemia > 200 mg/dl. Grado C |
| – Mannitolo – Furosemide – NO corticosteroidi (peggiorano outcome) |
Se presente un deterioramento dello stato di coscienza; Se segni neuroradiologici di erniazione obliterazione delle cisterne perimesencefaliche. Grado C |
| Diazepam Lorazepam |
Se crisi epilettica ripetuta. Grado C |
| Farmaci anti-aritmici Atropina |
Se sono presenti turbe del ritmo che determinano una instabilità emodinamica |
| – Furosemide – Nitroglicerina/ISDN – Dopamina |
Se presente un quadro di edema polmonare associato |
| Eparina a basso peso molecolare | Prevenzione trombosi venosa profonda |
| N.B.: Pz. allettato, possibili paralisi di importanti gruppi muscolari |
Una volta fatta la diagnosi etiologica di malattia cerebrovascolare, si può attuare la
terapia atta a correggere/eliminare la causa (se possibile) di quel quadro clinico.
Tab. 10 – Correzione delle cause nelle MCV
| Classificazione | Terapia e grado di raccomandazione |
|---|---|
| Emorragia subaracnoidea Emorragia epidurale |
Terapia neurochirurgica – Raccomandazione Grado A |
| Ictus emorragico | Terapia neurochirurgica se aggredibile |
| Ictus ischemico | – terapia antiaggregante (ASA, Ticlopidina, Dipiridamolo, Clopidogrel); terapia anticoagulante (se presente fibrillazione atriale) – Raccomandazione Grado A – terapia trombolitica in Italia solo in alcuni centri |
L’outcome del paziente con ictus non dipende solo da una corretta terapia della fase
acuta, ma migliora se già dall’inizio dell’ospedalizzazione si esegue un programma di
prevenzione delle disabilità che si attua perseguendo i seguenti obiettivi:
- mantenere un’adeguata nutrizione/idratazione (appena possibile valutare la capacità di deglutizione)
- salvare l’integrità della cute
- gestire la funzione vescicale ed evacuativa (togliere il catetere vescicale eventualmente inserito in emergenza appena possibile, mantenere alvo regolare)
- eseguire la profilassi delle TVP
- trattare prontamente la febbre e riconoscere rapidamente le infezioni respiratorie e
trattarle
Il Pz. plegico o con danni alla motilità volontaria tende ad assumere delle posture
patologiche.
Cosa fare:
- controllare l’allineamento del corpo
- variare le posture ogni 2-3 ore
- dotare di materasso antidecubito ed archetto alza coperte
- accostarsi dal lato plegico
Cosa non fare:
- lasciare in posizione scorretta
- applicare fleboclisi agli arti plegici
- eseguire mobilizzazioni brusche (trauma!)
- trazionare la spalla dell’arto plegico durante il nursing, i trasferimenti, le rotazioni
- stimolare pianta del piede ed il palmo della mano
- dotare di pallina da stringere
Piano assistenziale infermieristico delle malattie cerebrovascolari
Ingresso
Problema: Accertamento diagnostico
- Obiettivo: collaborare con il personale medico all’accertamento diagnostico
- Interventi
- valutare stato di coscienza (Glasgow coma scale)
- rilevare parametri vitali (PA – F.C. -F.R – Sat. O2- T.C.)
- spogliare il paziente
- assicurare accesso venoso (non utilizzare lato plegico-catetere grosso calibro)
- eseguire prelievo esami ematici + test rapido glicemia/invio urgente e ritiro referti
- eseguire ECG (se possibile monitorizzare paziente)
- EGA
- gestire paziente per esecuzione TAC senza MdC: se cosciente e collaborante invio c/o
servizio TAC senza assistenza – se non collaborante invio c/o servizio TAC con assistenza infermieristica – se in coma o incubato invio al servizio Tac con assistenza rianimatoria - Gestire paziente per esecuzione Rx torace
- Interventi
Le prime 48 ore
Problema: Possibile comparsa di complicanze correlate (cardiologiche-ipossiemia-ipo/ipertensione-iperpiressia-infezioni-squilibri elettrolitici/disidratazione. TVPneurologiche-motorie)
- Obiettivo: gestire o ridurre al minimo le complicanze
- Interventi
- posizionare paziente supino con testata del letto elevata di 30° rispetto al piano del
letto, evitare spostamenti rapidi. Riduce congestione cerebrovascolare – evita
ab ingestis - posizionare monitor ECG per monitoraggio continuo (qualora ciò non sia possibile
programmare controlli ripetuti di ECG: 2-4 volte al giorno). Nelle prime 48
ore. - posizionare monitor per rilevazione parametri vitali (Fc-Fr-PA). Mettere allarmi di minima e massima (PA non > 185- 220 mm Hg – sistolica – e non > 105-120 mmg Hg – diastolica –). Modificazioni del polso possono riflettere ipertensione endocranica (bradi o tachicardia), rilevare modificazione del ritmo respiratorio (rallentamento del ritmo con o meno presenza di apnee); l’aumento della PA dovrebbe essere rilevato con sfigmomanometri automatici e riferiti immediatamente al medico per istituire terapia come da protocolli
- posizionare saturimetro per controllo continuo stato di ossigenazione ematica (almeno prime 24 ore)+ eventuale somministrazione di ossigeno se Sat. O2 < 92%(ipossiemia)- iniziare con somministrazione di O2 -4 l/min. Se ipossiemia moderata. Mantenere SATO2>92%, non è indicato somministrare O2 routinariamente nei pazienti con ictus.
- monitorare TC ogni 6 ore nei primi gg. e somministrare paracetamolo o utilizzare mezzi fisici di raffreddamento per mantenere TC < 37°C 6). Mantenere TC
< 37°C (l’ipotermia ha un effetto neuroprotettivo) - controllare glicemia capillare ogni 6 ore e somministrare insulina rapida se glicemia > 200 mg/dl 7). ) L’iperglicemia è un fattore negativo al pari della ipertermia –anche l’ipoglicemia può essere un fattore aggravante il danno ischemico
- valutare stato di idratazione del paziente/bilancio idro-elettrolitico. Una buona idratazione serve a ridurre la viscosità ematica e migliora il flusso ematico cerebrale.
- posizionare CV solo in presenza di grave disfunzione vescicale (valutare caso per caso)/cateterismo ad intermittenza. Valutare globo o residuo post-minzionale ed intervenire con cateterismo sterile ad intermittenza
- posizionare SNG se paziente con vomito e coscienza limitata
- posizionare il paziente su presidio antidecubito adeguato (vedi protocollo) /cambiare posizione ogni 2 ore evitando traumi da stiramento su arto plegico e sulla spalla in particolare/mantenere il corretto allineamento corporeo. Previene lesioni da pressione – evita posizioni in flessione o estensione degli arti.
- praticare terapia come da prescrizione medica e protocolli. La terapia infusionale è rivolta al trattamento dei disturbi pressori (ipo/ ipertensione) e comporta controlli periodici ravvicinati
- posizionare paziente supino con testata del letto elevata di 30° rispetto al piano del
- Interventi
Dopo le 48 ore
Problema: Possibile comparsa di complicanze a livello urinario, polmonare, neuropsicologiche, malnutrizione, LDD, TVP, cadute, danni articolari
- Obiettivo: gestione e prevenzione complicazioni
- Interventi
- posizionare C V solo in presenza di grave disfunzione vescicale (valutare
caso per caso)/cateterismo ad intermittenza o altri accorgimenti, eseguire manovre in asepsi, mantenere adeguata idratazione, attuare controllo della
diuresi e favorire dieta adeguata - posizionare correttamente la persona, eseguire fisioterapia respiratoria precoce, aspirazione vie aeree superiori, prevenzione ab ingestis
- supportare la persona ed i familiari per prevenire situazioni caratteristiche
quali la depressione, l’alienazione, le reazioni emotive esagerate (riso/
pianto/reazioni catastrofiche) - valutare se presenza di disfagia, praticare nutrizione enterale (OS – SNG
-PEG), praticare nutrizione parenterale, valutare periodicamente stato nutrizionale. La malnutrizione proteico-energetica è frequente;
evitarla previene le complicanze, riduce i tempi di ospedalizzazione, migliora la qualità di vita - prevenire disabilità: mobilizzazione (almeno 3-4 volte al giorno) ed interventi riabilitativi precoci, posturare correttamente gli arti per evitare malposizionamenti, promuovere verticalizzazione precoce attraverso l’acquisizione della posizione seduta entro il terzo giorno (se non controindicato). Evita malposizionamenti, riduce rischio LDD
- prevenire cadute valutando attentamente pazienti a rischio, adottare mezzi protettivi adeguati (giubbotti anticaduta da letto e/o sedia), eliminare cause ambientali, aiutare la persona negli spostamenti ed accompagnarla al bagno ad intervalli regolari, istruire familiari e pazienti sul comportamento consono
da adottare. In situazioni di emergenza (per proteggere il paziente e gli operatori) la contenzione può essere effettuata ma l’indicazione medica deve essere ottenuta
entro breve. La contenzione va sempre preceduta da un’attenta valutazione dello stato del Pz., dei fattori ambientali, temporali ecc. Intervenire con interventi meno restrittivi, coinvolgere il Pz., o i suoi familiari nel processo decisionale (consenso). Specificare sempre il tempo di inizio e fine contenzione. La durata deve essere al
massimo di 24 ore (eventuale ulteriore prescrizione); durante la contenzione il Pz. deve essere controllato ogni 30 minuti e verrà rilasciato al massimo ogni 2 ore
- posizionare C V solo in presenza di grave disfunzione vescicale (valutare
- Interventi
Fonti bibliografiche
- STROKE 2004; 35: 520-527
- BUCCELLETTI F., MAZZONE M., PORTALE G. ET AL, Trattamento precoce dell’ictus ischemico linee guida e revisione della letteratura, in “GIMUPS” 2003; 5: 29-34
- SPREAD, Ictus cerebrale: linee guida italiane, Stesura del 4.3.2003, Pubblicazioni Catel –
Hyperphar Group SpA, Milano, 2003 - www.spread.it
Questo capitolo (Autrici Laura Baffoni, Anna Maria Gugnali) è tratto dal volume “Medicina d’urgenza per l’infermiere – Percorsi clinici ed assistenziali” a cura di Mario Marzaloni – ed. Maggioli 2005 – Fuori produzione.
Leggi anche:
https://www.dimensioneinfermiere.it/shock-gestione-infermieristica/



















Scrivi un commento
Accedi per poter inserire un commento